Из статьи вы узнаете, что такое острый лимфобластный лейкоз (ОЛЛ), симптомы и причины патологии, особенности диагностики и лечения заболевания.
Общая информации
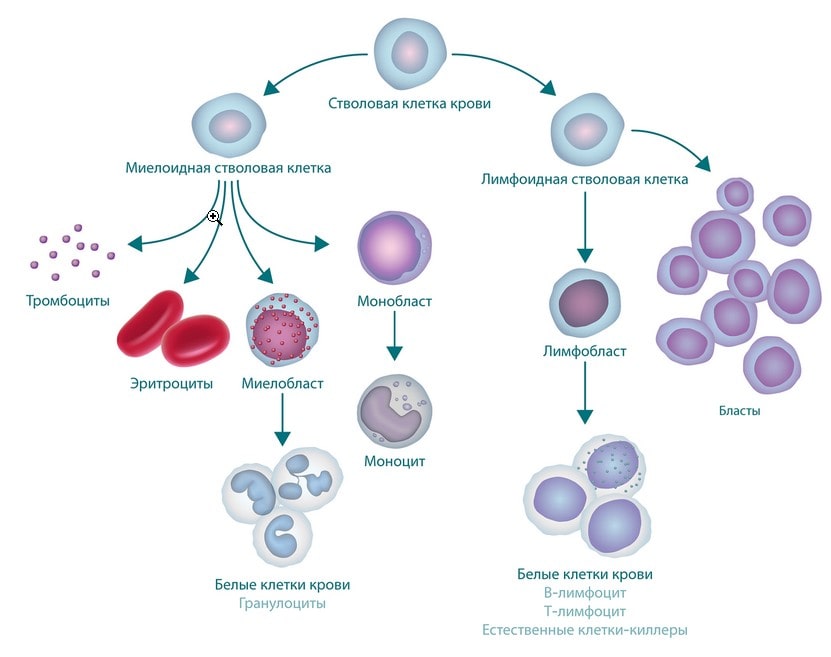
Острый лимфобластный лейкоз (ОЛЛ) является наиболее частым онкологическим заболеванием у детей, но поражает также и взрослых всех возрастов. Злокачественная трансформация и неконтролируемая пролиферация аномально дифференцированных, долго живущих гемопоэтических клеток-предшественниц приводит к появлению большого количества циркулирующих бластных клеток, замещению нормального костного мозга опухолевыми клетками и возможности лейкемической инфильтрации ЦНС и яичках.
Симптомы включают утомляемость, бледность, инфекции, боли в костях, симптомы расстройства ЦНС (например, головная боль), склонность к подкожным кровоизлияниям и кровотечениям. Диагноз в большинстве случаев можно поставить на основании изучения мазка периферической крови и костного мозга.
Лечение обычно включает комбинированную химиотерапию до достижения ремиссии, интратекальную и системную химиотерапию и/или кортикостероиды для профилактики расстройств ЦНС, иногда черепно-мозговое облучение, направленное на интрацеребральной лейкозный инфильтрат, консолидирующую химиотерапию с трансплантацией стволовых клеток или без нее и поддерживающую химиотерапию в течение до 3 лет во избежание рецидива.
Частота встречаемости и факторы риска ОЛЛ
На долю ОЛЛ приходится 75-80% всех опухолевых заболеваний кроветворной системы у детей (3-4 случая на 100 тысяч детей в год). Именно ОЛЛ – самое распространенное онкологическое заболевание у детей. Чаще всего ОЛЛ возникает в возрасте до 14 лет; пик детской заболеваемости приходится на возраст 2-5 лет. У мальчиков эта болезнь встречается немного чаще, чем у девочек.
Вероятность возникновения ОЛЛ несколько повышена у людей, ранее получавших лечение от какой-либо другой болезни (обычно злокачественной опухоли) с использованием облучения или определенных видов цитостатической химиотерапии. Также риск ОЛЛ повышен у детей с некоторыми генетическими нарушениями – например, с синдромом Дауна, нейрофиброматозом типа I или первичными иммунодефицитными состояниями.
Риск заболеть для ребенка выше среднего, если у его брата- или сестры-близнеца уже был диагностирован лейкоз.
Впрочем, в большинстве случаев ОЛЛ не удается обнаружить никакого из перечисленных факторов риска, и причины, вызвавшие болезнь, остаются неизвестными.
По статистике в Германии в Детском Раковом Регистре (г. Майнц) ежегодно регистрируется около 500 детей и подростков в возрасте от 0 до 14 лет с диагнозом ОЛЛ. А общее количество заболевших в возрасте до полных 18 лет ежегодно составляет примерно от 550 до 600 человек. Заболеть ОЛЛ можно в любом возрасте, то есть взрослые также могут заболеть. Но чаще всего острый лимфобластный лейкоз встречается всё же у детей в возрасте от года до пяти лет. А мальчики болеют немного чаще, чем девочки.
Признаки и симптомы острого лимфобластного лейкоза
ОЛЛ характеризуется множеством различных признаков и у разных больных может проявляться совершенно по-разному. Большинство наблюдаемых симптомов, однако, обусловлено тяжелыми нарушениями кроветворения: избыток аномальных бластных клеток при ОЛЛ сочетается с недостаточным количеством нормальных функциональных клеток крови.
Обычно наблюдаются слабость, бледность, снижение аппетита, потеря веса, учащенное сердцебиение (тахикардия) – проявления анемии и опухолевой интоксикации. Недостаток тромбоцитов проявляется мелкими кровоизлияниями на коже и слизистых оболочках, кровотечениями из десен, носовыми и кишечными кровотечениями, кровоподтеками, синяками. Из-за накопления бластных клеток часто увеличиваются лимфоузлы – в частности, шейные, подмышечные, паховые. Нередко увеличиваются также печень и селезенка — как говорят, возникает гепатоспленомегалия.
Часто наблюдаются боли в костях и суставах, иногда возникают патологические (то есть вызванные заболеванием) переломы костей. Из-за недостаточного количества нормальных зрелых лейкоцитов возможны частые инфекции. Повышение температуры может наблюдаться как в связи с возникшей на фоне лейкоза инфекцией, так и из-за опухолевой интоксикации. Иногда одним из проявлений острого лейкоза является продолжительная ангина, плохо поддающаяся терапии антибиотиками.
В некоторых случаях ОЛЛ вызывает изменения и в других органах: глазах, почках, яичках у мальчиков и яичниках у девочек, причем у мальчиков поражение половых органов наблюдается чаще. Нередко возникает поражение центральной нервной системы — нейролейкемия.
Так как все наблюдаемые симптомы могут быть связаны и с другими заболеваниями и не специфичны для ОЛЛ, перед началом лечения необходима лабораторная диагностика, которая в срочном порядке производится в больничных условиях.
Какие бывают формы ОЛЛ?
Когда ребёнок заболевает ОЛЛ, то это значит, что в организме произошла мутация (злокачественное изменение) незрелых клеток-предшественников лимфоцитов. Клетки-предшественники (или клетки-родоначальники) могут поломаться (мутировать) в любой момент, когда клетка ещё созревает. То есть когда молодая клетка растёт, она проходит через разные ступени созревания, и поломаться она может на любой ступени своего созревания. Это значит, что мутировать могут не только разные подгруппы лимфоцитов, но и поломки происходят в любой начальный этап роста клетки. Именно по этой причине у заболевших детей находят разные формы ОЛЛ.
Например, все так называемые формы В-ОЛЛ (врачи также могут говорить о В-клеточном или В-линейном лейкозе) произошли из клеток-предшественников В-лимфоцитов. А все так называемые формы Т-ОЛЛ (врачи также могут говорить о Т-клеточном или Т-линейном лейкозе) появились из клеток-предшественников Т-лимфоцитов. Если мутация произошла на самом раннем этапе созревания клетки, то в названии формы болезни обязательно есть приставка «пре». Различают следующие формы или подтипы ОЛЛ:
- пре-пре-B-клеточный ОЛЛ (сегодня его чаще всего называют про-В ОЛЛ; также этот вариант могут обозначать как В-I или про-B-клеточный ОЛЛ, или нуль-клеточный ОЛЛ)
- B-II ОЛЛ (или «обычного» типа)
- пре-B-клеточный (B-III) ОЛЛ
- зрелоклеточный (B-IV) ОЛЛ
- про- и пре- Т-клеточный ОЛЛ
- кортикальный Т-клеточный ОЛЛ
- зрелый T-клеточный ОЛЛ
Важно знать, что сама болезнь — ОЛЛ — имеет разные формы или подварианты. Друг от друга они сильно отличаются, то есть болезнь может протекать совершенно по-другому и шансы на выздоровление (на языке специалистов — прогноз) тоже разные. Когда врачи решают, как именно они будут лечить больного ребёнка, они обязательно учитывают все различия и специфику.
Почему дети заболевают ОЛЛ?
Никто точно не знает, почему дети заболевают острым лимфобластным лейкозом (ОЛЛ). Известно, что ребёнок заболевает, когда ещё не созревшая клетка–предшественник лимфоцитов начинает злокачественно изменяться. С этих повреждений начинается генетическая мутация клетки. Но чаще всего остаётся непонятным, почему произошли генетические изменения, и почему одни дети с такими изменениями заболели, а другие — нет.
Например, у детей, заболевших ОЛЛ, есть генная мутация, которую находят уже у новорожденного. Но ребёнок заболевает только годы спустя. При этом не каждый ребёнок с такой генной мутацией заболевает ОЛЛ. Это говорит о том, что есть не только генетическая предрасположенность, но и другие внешние причины. По всей вероятности, дети заболевают тогда, когда одновременно совпали несколько разных факторов риска.
Известно, что у детей и подростков с определённым врождённым или приобретённым иммунодефицитом [дефекты иммунитета], или если у них есть определённые хромосомные отклонения (например, синдром Дауна или анемия Фанкони), есть высокая предрасположенность заболеть одной из форм лимфобластного лейкоза. Также определённое влияние на то, что начинается лейкоз, могут оказывать радиация и рентгеновское излучение, некоторые химические вещества и медикаменты, а также определённые вирусы. Но не у каждого ребёнка можно точно понять, что именно послужило причиной болезни.
Диагностика
При ОЛЛ возникают изменения в обычном клиническом анализе крови: понижены уровни эритроцитов и тромбоцитов, появляются бластные клетки. Очень высокий лейкоцитоз возможен, но, вопреки распространенному мнению, наблюдается не во всех случаях. В целом же надежно поставить диагноз можно только при исследовании образца костного мозга; для этой цели необходима костномозговая пункция.
При морфологическом исследовании диагноз «острый лимфобластный лейкоз» ставится при обнаружении более 25% бластных клеток в костном мозге (в противном случае речь может идти о лимфобластной лимфоме). Но обязательно производятся более тонкие исследования: цитохимическое (окрашивание клеток, позволяющее более точно установить их природу), цитогенетическое (изучение строения хромосом в лейкемических клетках), иммунофенотипирование (изучение белковых молекул на поверхности клеток). Дело в том, что при диагностике очень важно не только надежно отличить ОЛЛ от острого миелоидного лейкоза, но и определить конкретный вариант ОЛЛ, поскольку он сильно влияет на терапию и прогноз заболевания.
Так, ОЛЛ может быть B-клеточным (около 80% случаев) и T-клеточным, в зависимости от того, относятся ли лейкемические клетки к B- или T-лимфоцитарной линии. В зависимости от «степени зрелости» бластных клеток среди как В-, так и Т-клеточных лейкозов выделяют несколько вариантов; их установление в ходе иммунофенотипирования важно для определения стратегии лечения. Все большую важность для определения терапии приобретают и генетические особенности опухолевых клеток.
В ходе диагностики ОЛЛ также необходимо исследовать состояние центральной нервной системы. Анализ спинномозговой жидкости (ликвора) позволяет определить, нет ли у больного поражения центральной нервной системы – нейролейкемии. Образец ликвора для анализа получают посредством пункции спинномозгового канала.
Возможны и дополнительные диагностические процедуры для исследования пораженных лимфоузлов и внутренних органов – компьютерная томография (КТ), ультразвуковое исследование (УЗИ) и так далее.
Диагностические исследования позволяют для каждого конкретного больного определить ту или иную группу риска, от которой зависят прогноз заболевания и планируемое лечение. Так, говорят о стандартном риске, высоком риске и т.д. Отнесение к той или иной группе зависит от многих факторов. Перечислим некоторые из них.
- Возраст больного: менее благоприятным считается возраст до 1 года или старше 10 лет.
- Количество лейкоцитов: риск увеличивается при очень высоком лейкоцитозе в момент диагноза.
- Т-клеточный ОЛЛ у детей традиционно считается связанным с несколько более высоким риском по сравнению с В-клеточным.
- Хромосомные аномалии в лейкемических клетках, связанные с числом хромосом и транслокациями. При некоторых из них усложняется лечение болезни. Так, филадельфийская хромосома – транслокация t(9;22) – требует подключения дополнительных таргетных лекарств к терапии. Транслокация t(4;11) часто требует трансплантации костного мозга. В то же время, например, транслокация t(12;21) чаще всего связана с относительно хорошим прогнозом.
- Распространение ОЛЛ в другие органы, помимо костного мозга (например, возникновение нейролейкемии), определяет более высокий риск.
- При раннем или повторном рецидиве лейкоза риск значительно повышается.
Особенности лечения
Лечение острого лимфобластного лейкоза (ОЛЛ) проводится в два этапа. Первый этап заключается в уничтожении лейкемических клеток, находящихся в крови с достижением ремиссии заболевания. На втором этапе выполняется уничтожение остаточного заболевания для профилактики возникновения рецидива.
На каждом этапе, как правило, проводится профилактическая химиотерапия центральной нервной системы (CNS sanctuary therapy). При этом виде лечения химиопрепараты направляются непосредственно в мембраны, окружающие спинной мозг для того чтобы достичь лейкемических клеток, что невозможно при проведении обычной химиотерапии.
Параллельно может проводиться системная химиотерапия, направленная на уничтожение злокачественных клеток во всех частях организма или местная химиотерапия, направленная на уничтожение злокачественного процесса в каких-либо отдельных частях тела.
Химиотерапия с трансплантацией стволовых клеток
Такой метод лечения острого лимфобластного лейкоза позволяет проводить более агрессивную противоопухолевую терапию с более высокими дозами химиопрепаратов и/или облучения. При таком виде лечения, проводимом в стационаре, уничтожаются не только злокачественные клетки миеломы, но и здоровые клетки кроветворной системы, находящиеся в костном мозге. После их уничтожения производится пересадка здоровых стволовых клеток путём инфузии через крупную вену на шее или груди пациента. В дальнейшем из пересаженных здоровых стволовых клеток, которые могут быть аутологичными (забранными из здоровых частей собственного организма пациента) либо аллогенными (полученными от донора) образуются здоровые клетки крови.
Пациенты с ОЛЛ, плохо переносящие лечение
Около трети пациентов с острым лимфобластным лейкозом составляют пожилые люди (> 65). У пожилых пациентов с ОЛЛ чаще всего встречаются предшественники B-клеток, также они имеют более высокий риск нарушения и более сложные цитогенетические комплексы, включая положительую филадельфийскую хромосому (Ph+) или транслокацию t(v;11q23), а также нарушение при перестроенном гене недифференциированного лейкоза MLL (KMT2A).
Некоторые, однако не все, пожилые пациенты могут переносить стандартную индукционную терапию. Последующие схемы лечения (профилактика нарушений ЦНС, консолидация или интенсификация после ремиссии, а также поддерживающая терапия) зависят от сопутствующих заболеваний и состояния пациента. Например, пациенты пожилого возраста с несколькими сопутствующими заболеваниями, а также со слабыми показателями состояния здоровья могут проходить щадящую индукционную терапию без режима консолидации или поддерживающего лечения. У пожилых пациентов с Ph+ ОЛЛ применение ингибиторов тирозинкиназы (например, иматиниба, дазатиниба) в комплексе с кортикостероидами, назначаемых либо с низкой интенсивностью, либо без химиотерапии, приводило к 95–100% частоте полной ремиссии с 45–50%-ной безрецидивной выживаемостью в течение 2 лет и около 70%-ной двухлетней общей выживаемостью. Для пожилых пациентов с ОЛЛ при первой полной ремиссии вариантом является немиелоабляционная или алогенная мини- трансплантация гемопоэтических стволовых клеток.
Целевые иммунотерапевтические препараты, доступные для лечения рецидивирующего или рефрактерного ОЛЛ все чаще используются для лечения пожилых пациентов с ОЛЛ в клинических испытаниях или клинической практике.
Пожилые пациенты с ОЛЛ, вероятно, переносят применение аспарагиназы хуже, чем молодые пациенты.
Рецидивирующий или рефрактерный ОЛЛ
Лейкозные клетки могут повторно появиться в костном мозге, ЦНС, яичках и в других органах. Наиболее опасен костномозговой рецидив. Хотя новый курс химиотерапии приводит к второй ремиссии у большинства детей и около трети взрослых, последующие ремиссии, как правило, недолгие. При химиотерапии лишь небольшая часть больных с ранним костномозговым рецидивом достигает длительной безрецидивной вторичной ремиссии или излечения.
Новые подходы к иммунотерапии показывают впечатляющие результаты при рецидивирующем/рефрактерном ОЛЛ. Антитела, такие как блинатумомаб, которые приносят Т клетки к лейкозным бластам, показывают эффективность при рецидивирующем ОЛЛ. Химерный антигенный рецептор Т-клеток (CAR-T), созданный и полученный от Т-клеток пациента, успешно вызывает ремиссию у пациента с рецидивом ОЛЛ, хотя и обладает существенной токсичностью (2).
Доступные сеансы иммунотерапии для рецидивирующего или рефрактерного ОЛЛ включают
- Блинатумомаб
- Инотузумаб озогамицин
- Тисагенлеклейсел
Блинатумомаб, биоспецифический CD19-направленный активатор CD3 T-клеток, продлевает общую выживаемость у детей и взрослых с рецидивирующим или рефрактерным пре-B-клеточным ОЛЛ, будь то Ph+ или Ph-. Опасные для жизни токсические эффекты могут включать синдром высвобождения цитокинов и симптомы токсического поражения нервной системы (например, судороги, энцефалопатию с нарушением сознания и нарушением речи, координации и/или равновесия). Может потребоваться прерывание или прекращение использования блинатумомаба с применением высокой дозы дексаметазона или без него. Наиболее распространенными неврологическими симптомами после применения блинатумомаба являются головная боль и тремор (3).
Инотузумаб озогамицин, CD22-направленное, нагруженное лекарством антитело с калихеамицином, также доступен для применения у взрослых с рецидивирующим или рефрактерным про-B-клеточным ОЛЛ. Одно из исследований показало, что частота ремиссии значительно выше после 1–2 циклов терапии инотузумаба озогамицином в сравнении со стандартной химиотерапией (4). Инотузумаб может вызывать гепатотоксичность, в том числе смертельные и угрожающие жизни веноокклюзионные заболевания, и его применение связано с более высокой смертностью после трансплантации, не зависящей от рецидива заболевания.
Тисагенлеклейсел, препарат CD19-направленной генетически модифицированной аутологичной Т-клеточной иммунотерапии, доступен для лечения пациентов в возрасте до 25 лет с ОЛЛ из В-клеточных предшественников в невосприимчивой форме, либо со вторым или с последующим рецидивами. Может возникнуть синдром высвобождения цитокинов, а также представляющая опасность для жизни или со смертельным исходом неврологическая токсичность (5).
Другие лекарства, которые на данный момент доступны, но для которых при этом клинически значимые результаты не были убедительно показаны, включают:
- Липосомный винкристин (алкалоид барвинка): для взрослых с Ph-негативным ОЛЛ, по крайней мере, во время 2-го рецидива или прогрессирования, несмотря на ≥ 2 курса противолейкозной терапии
- Клофарабин (аналог пуринового нуклеозида): для пациентов в возрасте от 1 до 21 года с рецидивирующим или рефрактерным ОЛЛ после ≥ 2 предыдущих схем
- Аналог пролекарственного препарата с использованием арабинозида гуанозида препарат неларабин (пуриновый нуклеозид): для Т-клеток ОЛЛ, которые не дают ответа, или рецидив которых произошел после ≥ 2 предыдущих схем лечения.
Трансплантация стволовых клеток при наличии HLA-идентичных сиблингов после индукционной химиотерапии или иммунотерапии дает самую большую вероятность достижения долгосрочной ремиссии или излечения. Иногда используются клетки от других родственных доноров или от совместимых с реципиентом доноров, несовместимых с реципиентом доноров. Трансплантация редко используется для пациентов > 65 лет, потому что вероятность успешного исхода очень мала, а побочные эффекты, скорее всего, будут смертельными.
При рецидивах с поражением ЦНС применяется интратекальное введение метотрексата (с или без цитарабина или кортикостероидов) дважды в неделю до исчезновения всех симптомов. Роль продолжительного применения интратекальных препаратов и облучения ЦНС остается неясной.
Рецидив в яичках может клинически проявляться безболезненным плотным увеличением тестикул или может быть выявлен при биопсии. При клинических признаках одностороннего поражения необходимо проведение биопсии непораженного яичка. Лечение включает лучевую терапию пораженного яичка и системную реиндукцию.
Поддерживающая терапия
Поддерживающее лечение при острых лейкозах сходно и может включать:
- Переливание крови
- Антимикробные препараты
- Гидратацию и ощелачивание мочи
- Психологическую поддержку
Трансфузии эритроцитов, а иногда тромбоцитов выполняются по показаниям больным с кровотечениями или анемией. Профилактическое переливание тромбоцитарной массы проводится при условии, если уровень тромбоцитов снижается до < 10000/мкл. При анемии (уровень гемоглобина < 7 или 8 г/дл) применяется трансфузия эритроцитарной массы. Трансфузия гранулоцитов обычно не используется.
Для профилактики и лечения часто необходимо использование антибиотиков в связи с тем, что у больных развивается иммуносупрессия, что может приводить к быстрому развитию инфекций без проявления обычной клинической картины. После проведения необходимых обследований и посева культур пациентам с лихорадкой и уровнем нейтрофилов < 500/мкл следует начинать лечение антибактериальными препаратами широкого спектра действия, воздействующими и на грамположительные и на грамотрицательные микроорганизмы (например, цефтазидим, пиперациллин и тазобактам, меропенем). Все чаще приходится сталкиваться с грибковыми инфекциями, особенно пневмониями; эти инфекции представляют собой проблему для диагностики, поэтому для обнаружения грибковой пневмонии необходимо раннее выполнение КТ органов грудной клетки (т. е. в течение 72 часов с момента появления нейтропенической лихорадки, в зависимости от степени уверенности в диагнозе). При неэффективности антибактериальной терапии в течение 72 часов необходимо назначение эмпирического противогрибкового лечения. Возникает выраженное лекарственное взаимодействие между винкристином, который обычно используется во всех схемах лечения ОЛЛ и противогрибковыми азолами. У больных с рефрактерным пневмонитом необходимо учитывать возможность развития инфицирования Pneumocystis jirovecii или вирусной инфекции, для чего необходимо выполнить бронхоскопию и бронхоальвеолярный лаваж и назначить соответствующее лечение. Позаконазол, противогрибковый препарат 2-го поколения, показан для первичной профилактики пациентам > 13 лет, которые из-за иммуносупрессии имеют высокий риск развития инвазивных инфекций, вызванных Aspergillus и Candida (например, реципиенты гематопоэтических стволовых клеток с реакцией «трансплантат против хозяина»). Для пациентов с лекарственной иммуносупрессией (например, при продолжительном применении кортикостероидов при лечении ОЛЛ) для профилактики P. jirovecii пневмонии назначаются триметоприм/сульфаметоксазол (TMP/SMX), дапсон, атовахон или пентамидин. Профилактика с применением препарата ацикловира или валацикловира, как правило, рекомендуется для всех пациентов.
Гидратация, ощелачивание мочи бикарбонатом натрия IV, использование аллопуринола или расбуриказы могут предотвратить, а также лечить развитие гиперурикемии, гиперфосфатемии, гипокальциемии и гиперкалиемии (т. е. синдром лизиса опухоли), которые вызваны быстрым лизисом опухолевых клеток при проведении начальной терапии при ОЛЛ. Гиперурикемия минимизируется при помощи назначения до начала химиотерапии аллопуринола (ингибитора ксантиноксидазы) или расбуриказы — в РФ не зарегистрирована (рекомбинантной уратоксидазы), которые уменьшают трансформацию ксантина в мочевую кислоту.
Психологическая поддержка может помочь больным и их семьям преодолеть шок от болезни и трудности лечения этого потенциально опасного для жизни заболевания.
Прогноз (исход) при лечении острого лимфобластного лейкоза
Около 98% детей с ОЛЛ достигают ремиссии через несколько недель после начала лечения.Более 90% детей с ОЛЛ могут выздороветь. Пациенты считаются выздоровевшими примерно через 5 лет ремиссии.
Коэффициент выживаемости для пациентов с ОЛЛ в группах низкого риска может составлять более 95%.
Если у пациента резистентная (не дающая ответа на лечение) или рецидивирующая форма ОЛЛ, врачи обсуждают дальнейшие варианты терапии.
Литература
- Berry DA, Zhou S, Higley H, et al: Association of minimal residual disease with clinical outcome in pediatric and adult acute lymphoblastic leukemia: a meta-analysis. JAMA Oncol 3(7): e170580, 2017. doi:10.1001/jamaoncol.2017.0580
- Lee DW, Kochenderfer JN, Stetler-Stevenson M, et al: T cells expressing CD19 chimeric antigen receptors for acute lymphoblastic leukaemia in children and young adults: a phase 1 dose-escalation trial. Lancet385(9967) :517–528, 2015.
- Kantarjian H, Stein A, Gökbuget N, et al: Blinatumomab versus chemotherapy for advanced acute lymphoblastic leukemia. N Engl J Med 376(9):836–847, 2017.
- Kantarjian HM, DeAngelo DJ, Stelljes M, et al: Inotuzumab ozogamicin versus standard therapy for acute lymphoblastic leukemia. N Engl J Med 375(8):740–753, 2016.
- Maude SL, Laetsch TW, Buechner J, et al: Tisagenlecleucel in children and young adults with B-cell lymphoblastic leukemia. N Engl J Med 378(5):439–448, 2018.

