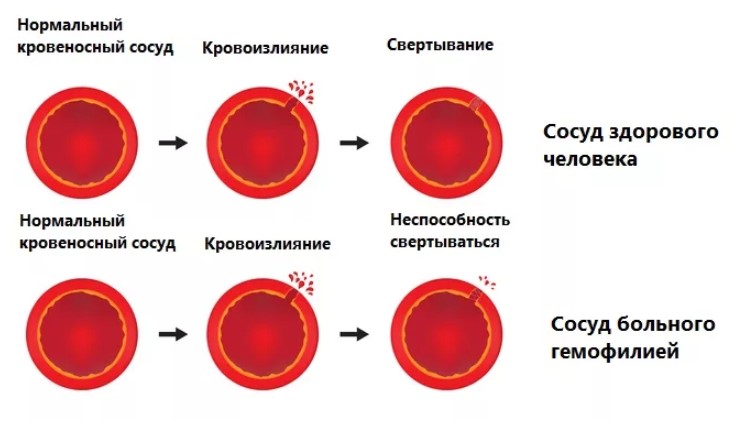
Гемофилия – это наследственная патология свертываемости крови (процесса коагуляции), из-за отсутствия факторов свертывания.
Общие данные
Впервые в письменных источниках о гемофилии упоминается в священной книге иудеев — талмуде. Около 15 веков назад так называемый «вавилонский талмуд» содержит запись об иудейском мальчике, не прошедшем обряд обрезания, так как оба его старших брата и трое двоюродных — по материнской линии умерли от потери крови после такой манипуляции.
В 12 веке Абу аль Касим, врач служивший при дворе одного из арабских правителей Испании, первым описал симптомы гемофилии. Он писал о нескольких семьях, в которых дети мужского пола умирали от небольших повреждений.
Современное научное исследование гемофилии ведется с XIX века. Впервые термин «гемофилия» был введен в 1828 году швейцарским врачом Хопфом.
Первой высокопоставленной носительницей гемофилии считается английская королева Виктория. В «наследство» от нее это заболевание было получено царствующими семьями Германии, Испании и России.
В России этот недуг часто называют «царским». Он известен из-за болезни Цесаревича Алексея — последнего наследника престола Российской империи.
Распространенность гемофилии А и В составляет 1 случай на 10000-50000 представителей мужского пола. Чаще всего дебют заболевания приходится на ранний детский возраст, поэтому гемофилия у ребенка является актуальной проблемой педиатрии и детской гематологии. Кроме гемофилии, у детей встречаются и другие наследственные геморрагические диатезы: геморрагическая телеангиэктазия, тромбоцитопатия, болезнь Гланцмана т. п.
Гемофилия А (недостаточность фактора VIII), которая поражает около 80% больных гемофилией, и гемофилия В (недостаточность фактора IX) имеют одинаковые клинические проявления и нарушения скрининг-теста. Оба заболевания являются генетическими нарушениями, сцепленными с Х-хромосомой. Специальные анализы факторов позволяют их различать.
Механизм развития
Для нормального гемостаза (см. рисунок Механизмы свертывания крови) требуется > 30% от нормального уровня факторов VIII и IX. Большинство пациентов с гемофилией имеют уровни < 5%; пациенты с тяжелой степенью заболевания имеют очень низкий уровень (<1%). Функциональный уровень (активность) фактора VIII или IX при гемофилии А и В, и, соответственно, степень тяжести кровотечения варьирует в зависимости от конкретной мутации в гене фактора VIII или IX.
У носителей этот уровень обычно достигает 50%; редко при случайной инактивации в ранней эмбриональной жизни нормальной Х-хромосомы уровень фактора VIII или IX у носителей становится менее 30%.
Большинство пациентов с гемофилией, которых лечили в начале 1980-х годов, были заражены ВИЧ-инфекцией в результате применения зараженной плазмы или концентратов фактора VIII или IX (до разработки эффективных вирусных инактиваторов). У некоторых больных вторично по отношению к ВИЧ-инфекции развилась иммунная тромбоцитопения, которая усугубляет кровотечение.
Причины гемофилии
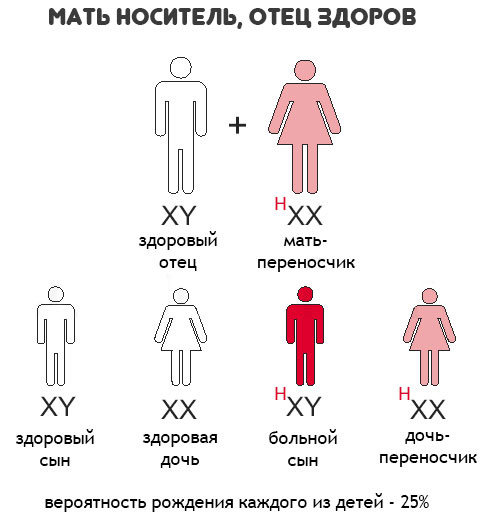
Гемофилия – наследственное заболевание, которое появляется в результате мутации, делеции или инверсии гена фактора VIII или фактора IX. Гемофилия поражает исключительно мужчин, т.к. эти гены расположены в Х-хромосоме. Носителями гена являются исключительно дочери мужчин с гемофилией, к сыновьям это не относится. Каждый сын носительницы гена имеет 50% шанс заболеть гемофилией, а каждая дочь с 50% вероятностью может стать носительницей.
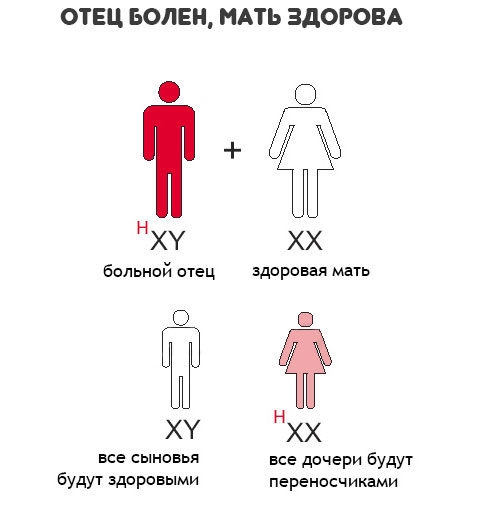
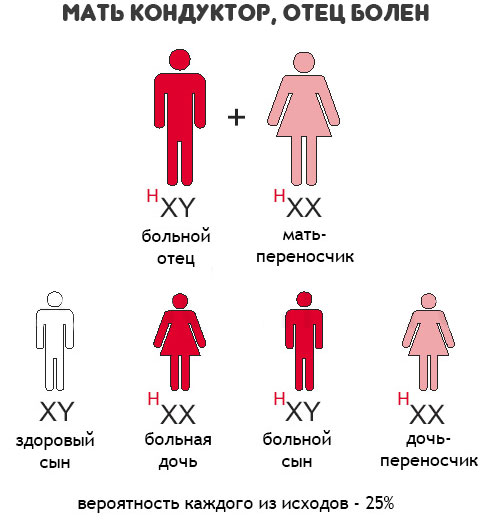
У здорового мужчины и женщины-кондуктора с одинаковой вероятностью могут родиться как больные, так и здоровые сыновья. От брака мужчины, больного гемофилией со здоровой женщиной рождаются здоровые сыновья или дочери-кондукторы. Описаны единичные случаи гемофилии у девочек, рожденных от матери-носителя и больного гемофилией отца.
Врожденная гемофилия встречается почти у 70 % пациентов. В этом случае наследуется форма и тяжесть гемофилии. Около 30% наблюдений приходится на спорадические формы гемофилии, связанные с мутацией в локусе, кодирующем синтез плазменных факторов свертывания крови на Х-хромосоме. В дальнейшем такая спонтанная форма гемофилии становится наследственной.
Свертываемость крови, или гемостаз, служит важнейшей защитной реакцией организма. Активизация системы гемостаза происходит в случае повреждения сосудов и начала кровотечения. Свертываемость крови обеспечивается тромбоцитами и особыми веществами – плазменными факторами. При дефиците того или иного фактора свертывания своевременный и адекватный гемостаз становится невозможным. При гемофилии в связи с дефицитом VIII, IX или других факторов нарушается первая фаза свертывания крови — образование тромбопластина. При этом увеличивается время свертывания крови; иногда кровотечение не останавливается в течение нескольких часов.
Классификация
Подразделение патологического процесса проводится по критерию недостаточной выработки фактора свертывания. Многое зависит от конкретной формы болезни. Всего по этому основанию выделают три ключевых вида.
- Типичная. Или классическая. Она же гемофилия А. Возникает примерно в 80% ситуаций. Обнаруживается у пациентов особенно часто. Симптоматика соответствует описываемой в литературе, когда говорят об общем правиле. Характеризуется скудным синтезом VIII фактора свертывания. Лечится с большим трудом, имеется возможность только устранить симптоматику и то на время и не полностью.
- Гемофилия Б. Вырабатывается мало фактора свертывания IX, что сказывается на скорости гемостаза. Также возможен вариант, когда это вещество не синтезируется вовсе. Принципиальных отличий с точки зрения пациента нет, поскольку клиника будет примерно той же, с некоторыми отличиями и значительными расхождениями с точки зрения объективных показателей. На долю этого типа приходится порядка 17% ситуаций.
- Гемофилия С. Редкая разновидность. Наблюдается всего у 2% пациентов. Плюс-минус. Отличительных черт не имеет, не считая лабораторных специализированных показателей.
Есть и другие типы нарушения, которые можно выделить по тому же критерию. Но они встречаются исключительно редко. Примерно в половине процента случаев. Потому имеют куда меньшую эпидемиологическую значимость.
Гемофилия у детей и взрослых классифицируется и по степени тяжести. Исходя из клиники, интенсивности необходимого провокатора, выделяют три основных разновидности расстройства.
- Легкая степень. Фактор вырабатывается в больших количествах, но его все же недостаточно. До определенного возраста пациент и его родители могут и не предполагать о наличии проблемы. Все вскрывается случайно. При получении тяжелой травмы, проведении операции и т.д. Интенсивность провокатора должна быть высокой. С такой формой патологического процесса человек вполне качественно и долго живет, имеет положительные прогнозы. Не всегда вообще требуется лечение.
- Средняя степень. Фактора синтезируется значительно меньше положенной нормы. Что заметно сказывается на состоянии человека. Если при легком течении изменение обнаруживается порой в подростковые годы, тут все понятно с начальных дней жизни пациента. Достаточно незначительного физического воздействия, чтобы спровоцировать кровоточивость. Такая форма нарушения трудно поддается коррекции. Однако прогнозы все же неплохие. При достаточной внимательности к собственному здоровью есть шансы на выживание.
- Тяжелая степень. Встречается часто. В том случае вообще нет необходимости во влиянии на тело извне. Нарушения настолько выраженные, что пациент становится жертвой кровотечений спонтанно, без видимых факторов. С точки зрения сохранения жизни, шансы невелики.
Обе классификации применяются для понимания сути болезни, разработки тактики терапии, выбора оптимальной схемы.
Симптомы патологии
Для пациентов с гемофилией характерны распространенные кровотечения в тканях (например, гемартрозы, мышечные гематомы, забрюшинные кровоизлияния). Кровотечение может быть быстрым или появляться медленно, в зависимости от степени травмы и уровня фактора VIII или IX. Боль часто возникает в самом начале кровотечения, иногда даже раньше других признаков кровотечения. Хронические или рецидивирующие гемартрозы могут привести к синовитам и артропатии. Даже несильный удар по голове может привести к внутричерепному кровотечению. Кровотечение в основании языка может привести к угрожающему для жизни сжатию дыхательных путей.
В случае легкой гемофилии (уровень фактора от 5 до 25% от нормы) сильное кровотечение может возникать при хирургическом вмешательстве или удалении зуба.
При умеренной гемофилии (уровни факторов от 1 до 5% от нормы) кровотечение возникает при наличии минимальной травмы.
Тяжелая форма гемофилии (уровень факторов VIII или IX менее 1% от нормы) вызывает тяжелые кровотечения в течение жизни, начиная с самого рождения (например, гематома волосистой части головы после родов или чрезмерное кровотечение после обрезания).
У новорожденных детей признаками гемофилии могут служить длительное кровотечение из культи пуповины, подкожные гематомы, кефалогематомы. Кровотечения у детей первого года жизни могут быть связаны с прорезыванием зубов, оперативными вмешательствами (инцизией уздечки языка, циркумцизио). Острые края молочных зубов могут стать причиной прикусывания языка, губ, щек и кровотечений из слизистых оболочек полости рта. Однако в грудном возрасте гемофилия дебютирует редко в связи с тем, что материнском молоке содержится достаточное количество активной тромбокиназы.
Вероятность посттравматических кровотечений значительно возрастает, когда ребенок с гемофилией начинает вставать и ходить. Для детей после года характерны носовые кровотечения, подкожные и межмышечные гематомы, кровоизлияния в крупные суставы. Обострения геморрагического диатеза случаются после перенесенных инфекций (ОРВИ, ветрянки, краснухи, кори, гриппа и др.) вследствие нарушения проницаемости сосудов. В этом случае нередко возникают самопроизвольные диапедезные геморрагии. Ввиду постоянных и длительных кровотечений у детей с гемофилией имеется анемия различной степени выраженности.
По степени убывания частоты кровоизлияния при гемофилии распределяются следующим образом: гемартрозы (70—80%), гематомы (10-20%), гематурия (14-20%), желудочно-кишечные кровотечения (8%), кровоизлияния в ЦНС (5%).
Гемартрозы являются наиболее частым и специфическим проявлением гемофилии. Первые внутрисуставные кровоизлияния у детей с гемофилией случаются в возрасте 1-8 лет после ушибов, травм или спонтанно. При гемартрозе выражен болевой синдром, отмечается увеличение сустава в объеме, гиперемия и гипертермия кожи над ним. Рецидивирующие гемартрозы приводят к развитию хронического синовита, деформирующего остеоартроза и контрактур. Деформирующий остеоартроз приводит к нарушению динамики опорно-двигательного аппарата в целом (искривлению позвоночника и таза, гипотрофии мышц, остеопорозу, вальгусной деформации стопы и др.) и к наступлению инвалидности уже в детском возрасте.
При гемофилии часто возникают кровоизлияния в мягкие ткани – подкожную клетчатку и мышцы. У детей обнаруживаются непроходящие синяки на туловище и конечностях, часто возникают глубокие межмышечные гематомы. Такие гематомы склонны к распространению, поскольку излившаяся кровь не сворачивается и, проникая вдоль фасций, инфильтрирует ткани. Обширные и напряженные гематомы могут сдавливать крупные артерии и периферические нервные стволы, вызывая интенсивные боли, паралич, атрофию мышц или гангрену.
Довольно часто при гемофилии возникают кровотечения из десен, носа, почек, органов ЖКТ. Кровотечение может быть инициировано любыми медицинскими манипуляциями (внутримышечной инъекцией, экстракцией зуба, тонзиллэктомией и др.). Крайне опасными для ребенка с гемофилией являются кровотечения из зева и носоглотки, поскольку могут привести к обструкции дыхательных путей и потребовать экстренной трахеостомии. Кровоизлияния в мозговые оболочки и головной мозг приводят к тяжелым поражениям ЦНС или летальному исходу.
Гематурия при гемофилии может возникать самопроизвольно или вследствие травм поясничной области. При этом отмечаются дизурические явления, при образовании кровяных сгустков в мочевыводящих путях — приступы почечной колики. У больных с гемофилией нередко обнаруживаются пиелоэктазия, гидронефроз, пиелонефрит.
Желудочно-кишечные кровотечения у пациентов с гемофилией могут быть связаны с приемом НПВС и др. лекарств, с обострением латентного течения язвенной болезни желудка и двенадцатиперстной кишки, эрозивным гастритом, геморроем. При кровоизлияниях в брыжейку и сальник развивается картина острого живота, требующая дифференциальной диагностики с острым аппендицитом, кишечной непроходимостью и др.
Характерным признаком гемофилии является отсроченный характер кровотечения, которое обычно развивается не сразу после травмы, а через некоторое время, иногда спустя 6-12 и более часов.
Диагностика
- Количество тромбоцитов, протромбиновое время, АЧТВ, анализы фактора VIII и IX
- Иногда уровень активности фактора Виллебранда, антиген и состав мультимера
Гемофилия диагностируется у пациентов с рецидивирующим кровотечением, необъяснимыми гемартрозами или продолжительным АЧТВ. Если у пациента подозревают тромбоцитопению, необходимо проведение анализов на определение количества тромбоцитов, протромбинового времени, АЧТВ, фактора VIII и IX. При гемофилии АЧТВ увеличивается, а протромбиновое время и количество тромбоцитов остаются в пределах нормы.
Анализы фактора VIII и IX помогают определить тип и степень тяжести гемофилии. Поскольку уровень фактора VIII также может быть снижен вследствие болезни Виллебранда (БВ), то у пациентов с только что диагностированной гемофилией А, особенно если гемофилия легкая и история показывает, что под влияние попадают и женщины, и мужчины семьи, измеряют уровень активности фактора Виллебранда (ФВ), его антиген и состав мультимера. Определение того, является ли женщина истинным носителем гемофилии А, иногда возможно путем измерения уровня фактора VIII. Кроме того, измерения уровня фактора IX часто идентифицирует носителей гемофилии B.
ПЦР-анализ ДНК, который включает в себя ген фактора VIII, может быть использован для выявления носителя гемофилии А и пренатальной диагностики гемофилии А по биопсии хориона в 12 недель или при амниоцентезе в 16 недель. Но риск выкидыша от таких процедур колеблется от 0,5 до 1%.
После многократного заместительного воздействия на фактор VIII или X почти у 30% больных гемофилией А и у 3% больных гемофилией В появляются изоантитела к фактору VIII или фактору IX (аллоантитела), которые блокируют активность коагулянта при каждом дополнительном введении фактора VIII или фактора IX. Таким образом, пациентов нужно исследовать на образование изоантител (например, путем измерения степени уменьшения АЧТВ сразу после смешивания плазмы пациента с равным объемом нормальной плазмы, а затем повторяя измерения после инкубации в течение 1 ч), особенно перед факультативными процедурами, которые требуют проведения заместительной терапии. Если изоантитела присутствуют, то их титры могут быть измерены путем определения степени снижения интенсивности фактора VIII при проведении серии разжижений плазмы пациента.
Диагностика гемофилии проводится при участии ряда специалистов: неонатолога, педиатра, генетика, гематолога. При наличии у ребенка сопутствующей патологии или осложнений основного заболевания проводятся консультации детского гастроэнтеролога, детского травматолога-ортопеда, детского отоларинголога, детского невролога и др.
Супружеские пары, находящиеся в группе риска по рождению ребенка с гемофилией, должны пройти медико-генетическое консультирование еще на этапе планирования беременности. Выявить носительство дефектного гена позволяет анализ генеалогических данных и молекулярно-генетическое исследование. Возможно проведение пренатальной диагностики гемофилии с помощью биопсии хориона или амниоцентеза и исследования ДНК клеточного материала.
После рождения ребенка диагноз гемофилии подтверждается с помощью лабораторных исследований гемостаза. Основные изменения показателей коагулограммы при гемофилии представлены увеличением времени свертывания крови, АЧТВ, тромбинового времени, МНО, времени рекальцификации; уменьшением ПТИ и др. Решающее значение при диагностике формы гемофилии принадлежит определению снижения прокоагулянтной активности одного из факторов свертывания ниже 50%.
При гемартрозах ребенку с гемофилией проводится рентгенография суставов; при внутренних кровотечениях и забрюшинных гематомах – УЗИ брюшной полости и забрюшинного пространства; при гематурии – общий анализ мочи и УЗИ почек и т. д.
Особенности терапии
Несмотря на то, что болезнь неизлечима, лечить гемофилию и контролировать состояние больного возможно. Пациенты получают инъекции недостающего фактора, отвечающего за свертываемость крови. Поэтому в зависимости от того, недостаток какого фактора в крови больного наблюдается, врач проводит лечение гемофилии:
- При типе «А» — в кровь вводится VIII фактор.
- При типе «В» — в кровь вводится IX фактор.
Все факторы свертываемости производят из крови, предоставляемой донорами или из крови выращенных специально для этого животных. Необходимая доза концентрата определяется степенью выраженности гемофилии, тяжестью и видом кровотечения.
В лечении гемофилии выделяют два направления – профилактические и «по требованию», в период проявлений геморрагического синдрома. Профилактическое введение концентратов факторов свертывания крови показано пациентам с тяжелой формой гемофилии и проводится 2-3 раза в неделю для предупреждения развития гемофилической артропатии и прочих кровотечений. При развитии геморрагического синдрома требуются повторные трансфузии препарата. Дополнительно используются свежезамороженная плазма, эритромасса, гемостатики. Все инвазивные вмешательства у больных с гемофилией (наложение швов, удаление зубов, любые операции) проводятся под прикрытием гемостатической терапии.
Если симптомы включают в себя кровотечение, то лечение необходимо начинать безотлагательно, даже если диагностические исследования еще не завершены. Например, лечение головной боли, которая может указывать на внутричерепное кровоизлияние, должно начаться до завершения КТ.
Замена недостающего фактора является первостепенной задачей.
При гемофилии А уровень фактора VIII должен быть поднят примерно:
- До 30% от нормы для предотвращения кровотечения после удаления зуба или во избежание начинающегося суставного кровотечения
- До 50% от нормы, если тяжелое суставное или внутримышечное кровотечение уже очевидно
- До 100% от нормы перед серьезным хирургическим вмешательством или если это внутричерепное, внутрисердечное или другое угрожающее для жизни кровотечение
Многократные вливания в размере 50% от изначально рассчитанной начальной дозы следует делать каждые 8–12 часов, чтобы сохранить минимальный уровень > 50% в течение 7–10 дней после серьезной операции или опасного для жизни кровотечения. Каждая единица/кг фактора VIII повышает уровень фактора VIII примерно на 2%. Таким образом, для повышения уровня от 0 до 50% потребуется около 25 единиц/кг.
Фактор VIII представляет собой очищенный концентрат фактор VIII, полученный от нескольких доноров. Он подвергается противовирусной обработке, но эта обработка не может полностью исключить парвовирус или вирус гепатита А. Рекомбинантный фактор VIII не содержит вирусов и обычно предпочтительнее, если только пациенты уже не являются носителями ВИЧ или вируса гепатита В или С.
При гемофилии B фактор IX может вводиться как очищенный, прошедший антивирусную обработку или рекомбинантный продукт каждые 24 ч. Показатели уровней коррекции коэффициента такие же, как и при гемофилии А. Однако для достижения этих уровней доза должна быть выше, чем при гемофилии А, поскольку фактор IX меньше, чем фактор VIII, и в отличие от VIII имеет широкое внесосудистое распределение.
Свежезамороженная плазма содержит факторы VIII и IX. Однако пока плазмаферез не будет сделан, как правило, пациентам с тяжелой формой гемофилии для увеличения фактора VIII или IX до уровней, на которых возможно избежать и проконтролировать кровотечение, цельную плазму не назначают. Таким образом, свежезамороженную плазму можно использовать только в случае необходимости проведения быстрой заместительной терапии при недоступности концентрата фактора или наличия у пациента коагулопатии, которая еще не определена точно.
Недавно сообщалось, что слитный белок рекомбинантного фактора VIII-Fc (1), слитный белок рекомбинантного фактора IX-Fc (2), полиэтиленгликоль (ПЭГ)-связанный рекомбинантный фактор VIII (3)и пегилированный фактор IX (4) с более продолжителным временем жизни в условиях in vivo обеспечивают успешный контроль кровотечения при гемофилии A и B.
В случае гемофилии А применяется эмицизумаб, который представляет собой рекомбинантное гуманизированное биспецифическое моноклональное антитело, которое связывается как с фактором IX, так и с фактором X, соединяя их в так называемый теназный комплекс, упоминаемый в публикациях на английском языке как «factor Xase-like active complex», что устраняет необходимость в факторе VIII и может быть эффективным средством лечения гемофилии A (5).
В клинических испытаниях для лечения гемофилии А или В среди более новых лекарственных средств присутствуют фитусиран и концизумаб (6, 7). Фитусиран в своем составе имеет ингибирующие молекулы РНК, которая снижает выработку природного антикоагулянтного белка – антитромбина. Концизумаб представляет собой гуманизированное моноклональное антитело, которое блокирует ингибитор пути тканевого фактора (TFPI), другие природные антикоагулянтные белки и, таким образом, увеличивает выработку тромбина при гемофилии А и В.
Генная терапия с использованием аденовирусного вектора для доставки гена фактора VIII или IX также подвергается клиническим испытаниям при лечении гемофилии А или В (8).
Как ФВ так и фактор VIII, сохраняются в тельцах Вейбеля-Палада эндотелиальных клеток и секретируются в ответ на стимуляцию эндотелиальных клеток (9). Дополнительная терапия при гемофилии А легкой или средней степени тяжести может, таким образом, включать in vivo стимуляцию эндотелиальных клеток пациента синтетическим аналогом вазопрессина DDAVP (дезамино-D- аргинин- вазопрессин, также известный как десмопрессин). Как указано при болезни Виллебранда, десмопрессин может временно повышать уровень фактора VIII. Перед использованием десмопрессина в терапевтических целях реакция больного на препарат должна быть проверена. Его использование после небольшой травмы или перед стоматологической хирургической операцией может заменить заместительную терапию. Десмопрессин может применяться только для больных с легкой формой гемофилии А (базисный уровень фактора VIII ≥ 5%), у которых наблюдается положительный ответ на лечение.
Антифибринолитический препарат (аминокапроновая кислота 2,5–4 г перорально четыре раза в неделю или транексамовая кислота 1,0–1,5 г перорально три или четыре раза в неделю) может также применяться как вспомогательная терапия при гемофилии А или В для предотвращения поздних кровотечений после удаления зубов или других травм слизистой оболочки ротоглотки (например, рваная рана языка).
При незначительных наружных кровотечениях (порезах, кровотечениях из полости носа и рта) может использоваться гемостатическая губка, наложение давящей повязки, обработка раны тромбином. При неосложненном кровоизлиянии ребенку необходим полный покой, холод, иммобилизация больного сустава гипсовой лонгетой, в дальнейшем – УВЧ, электрофорез, ЛФК, легкий массаж. Больным с гемофилией рекомендуется диета, обогащенная витаминами А, В, С, D, солями кальция и фосфора.
При правильной терапии, бережном отношении пациента к своему организму, длительность жизни гемофилика, не будет отличаться от продолжительности жизни человека без такой патологии.
Профилактика
Необходимо выявить членов семьи, которые являются носителями заболевания, и предложить им генетическую консультацию.
Для профилактики кровотечений больные гемофилией должны избегать применения аспирина и нестероидных противовоспалительных препаратов (оба вида препаратов замедляют тромбоцитарную функцию). Регулярный уход за полостью рта поможет избежать удаления зубов и других стоматологических хирургических вмешательств. Лекарства нужно принимать орально или внутривенно; после внутримышечных инъекций остаются гематомы.
Больных гемофилией нужно прививать против гепатита В.
Профилактика предполагает проведение медико-генетического консультирования супружеских пар, имеющих отягощенный семейный анамнез по гемофилии.
Дети, больные гемофилией, всегда должны иметь при себе специальный паспорт, где указан тип заболевания, группа крови и Rh-принадлежность. Им показан охранительный режим, профилактика травм; диспансерное наблюдение педиатра, гематолога, детского стоматолога и др. специалистов; наблюдение в условиях специализированного гемофильного центра.
Прогноз
Длительная заместительная терапия приводит к изоиммунизации, образованию антител, блокирующих прокоагулянтную активность вводимых факторов, и неэффективности гемостатической терапии в обычных дозах. В таких случаях больному с гемофилией проводится плазмаферез, назначаются иммунодепрессанты. Поскольку больным с гемофилией проводится частое переливание компонентов крови, не исключается риск инфицирования ВИЧ-инфекцией, гепатитами В, С и D, герпесом, цитомегалией.
Легкая степень гемофилии не влияет на продолжительность жизни; при тяжелой гемофилии прогноз ухудшается при массивных кровотечениях, обусловленных операциями, травмами.

